├Ültimas Not├Łcias
Anvisa: relator vota a favor de importação da Sputinik V e Covaxin
O relator do processo de importação das vacinas Sputnik V e Covaxin votou a favor da autorização excepcional e temporária
O relator do processo de importação das vacinas Sputnik V e Covaxin votou hoje (4) a favor da autorização excepcional e tempor├Īria para importação e distribuição dos imunizantes contra a covid-19. Durante reunião da Ag├¬ncia Nacional de Vigilância Sanit├Īria (Anvisa), Alex Machado Campos entendeu que estados e o governo federal podem utilizar os imunizantes, mas de forma controlada e cumprindo v├Īrias condicionantes para aplicação na população.
A votação continua. Até o momento, o placar da votação est├Ī 2 votos a 1 pelo uso restrito de doses das duas vacinas. No total, cinco diretores da Anvisa vão votar, inclusive o presidente, Antônio Barra Torres.
Pelo voto do relator, a importação dever├Ī ser restrita ao total de doses referente a 1% da população, e a aplicação dever├Ī ser destinada a maiores de 18 anos e menores de 60 anos. O uso por gestantes e pessoas com comorbidades não foi recomendado.
Além disso, a Anvisa dever├Ī ser comunicada sobre eventuais eventos adversos nas pessoas que forem imunizadas. Somente poderão ser utilizadas vacinas oriundas de f├Ībricas inspecionadas pela ag├¬ncia.
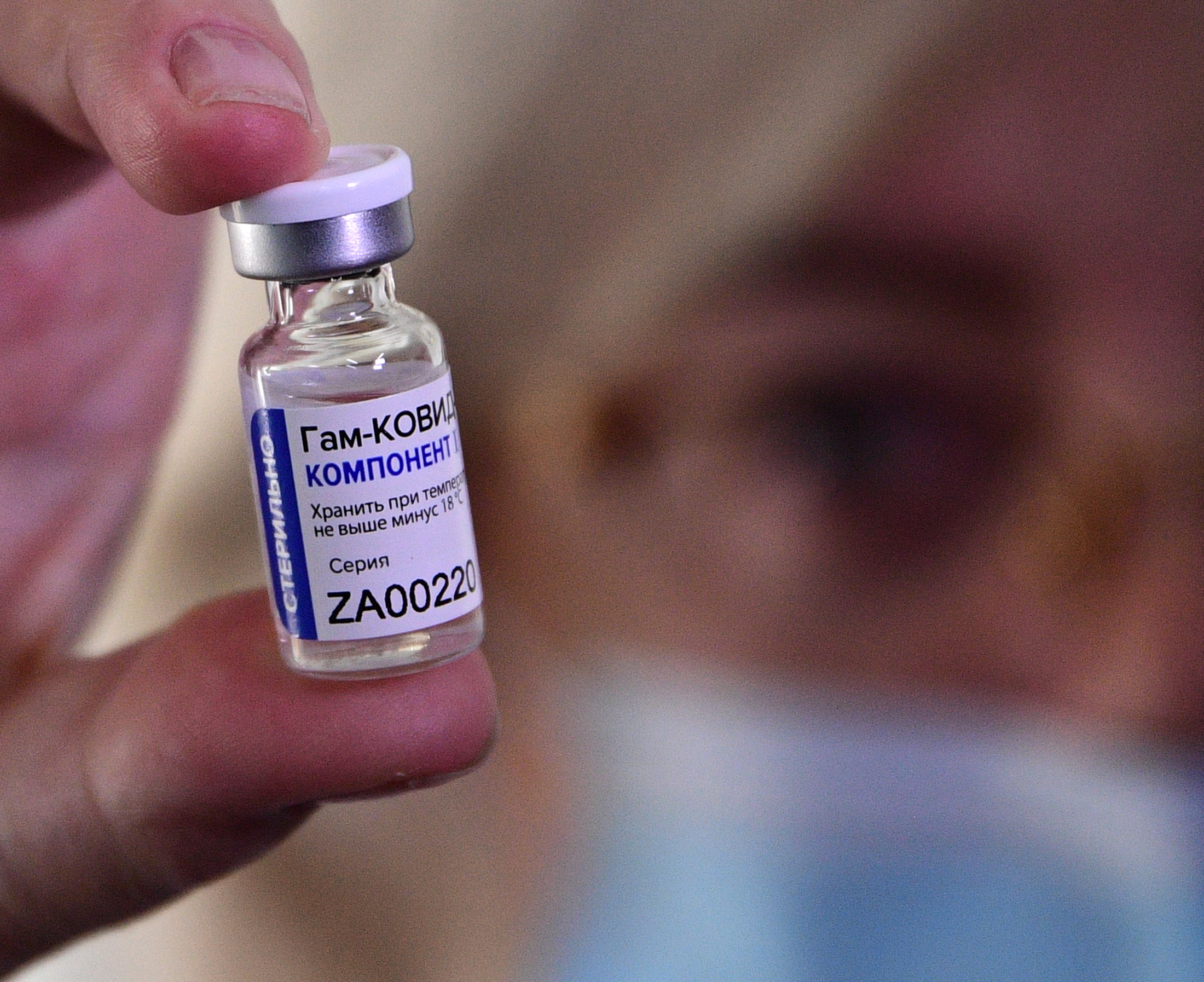
O caso é analisado em reunião da diretoria colegiada da ag├¬ncia para analisar pedidos dos estados da Bahia, de Sergipe, do Maranhão, de Pernambuco, do Cear├Ī e do Piaui para importação 37 milhões de doses da Sputnik V, produzida pelo Instituto Gamaleya, da R├║ssia. A compra de 20 milhões de doses da Covaxin, do laboratório indiano Bharat Biotech, foi feita pelo governo federal.
Campos disse que após a negativa da Anvisa para uso da Covaxin, as pend├¬ncias sobre as etapas de boas pr├Īticas na produção foram resolvidas. No caso da Sputnik V, após a decisão que rejeitou a importação , passou-se a admitir o uso do imunizante, mas com v├Īrias condicionantes, a partir da nova documentação apresentada por diversos governadores.
CEPAS
Para o relator, diante do surgimento de novas cepas e o agravamento da pandemia, a Anvisa deve promover a proteção da sa├║de da população, mitigando os riscos de segurança, efic├Īcia e qualidade dos imunizantes. "O contexto sanit├Īrio que nosso pa├Łs atravessa nos põe diante da necessidade de viabilizar o maior n├║mero de vacinas e medicamentos. Todo esforço se volta ao propósito de amenizar o sofrimento da população, abrandar ang├║stias dos gestores p├║blicos e combater o esgotamento de nossos profissionais de sa├║de", afirmou.
Fonte: Agência Brasil